‘본그로스’는 인체 뼈의 무기성분인 탄산아파타이트 소재의 합성 골 이식재로 ‘상악동 거상술’, ‘임플란트 식립 전 치조골 재건술’ 등에 사용되고 있으며 국내뿐만 아니라 태국, 인도네시아에 수출되고 있다.
‘본그로스’의 가장 큰 우수성은 특허기술1로 인정받은 뛰어난 기공률이다.
‘본그로스’는 골전도성을 극대화한 300㎛ 크기의 기공들을 입체적으로 연결한 다공성 구조의 합성 골 이식재로서 골 성장에 최적인 80% 이상의 기공률을 실현하여 골재생률이 우수하다는 평가다.
바이오알파 관계자는 “본그로스는 서울대병원, 서울아산병원, 삼성서울병원 등 유수 종합병원의 전임상 및 임상 시험에서 동종골 100%와 동등한 골 유합률이 입증됐다”면서 “골 형성이 완전해질 때까지 해면골의 구조와 부피 그대로 유효공간을 유지하기 때문에 이식부위 함몰 등의 우려가 없고 시술 후 주위 뼈 성장을 촉진해 자가 뼈 대체가 신속히 이뤄지도록 돕는다”고 설명했다.
또한 그는 “국제규격(ASTM F1185)의 초고순도 합성 뼈 무기성분을 1,200℃ 이상의 고온에서 굽고 감마선으로 멸균·제조해 FDA 기준에 맞춘 높은 안전성을 갖췄다”면서 “결핵이나 광우병 등 면역반응 및 감염성 질병의 발생이나 그로 인한 골유합의 지연 우려가 전혀 없다”고 덧붙였다.
‘본그로스’는 한국화학시험연구원 등 국내 공인기관 및 미국 GLP 인증기관인 Nelson laboratory의 엄격한 생물학적 안전성 시험에도 모두 통과한 것으로 알려지고 있다.
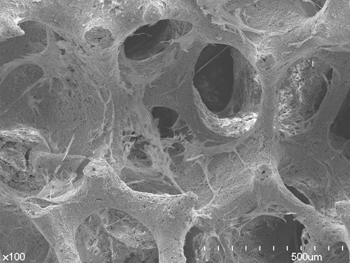
한편, ‘본그로스’는 멸균제품으로 필요 시 바로 시술 할 수 있으며, 자가골과 혼합해 사용 가능하다.
또한 실온보관으로 취급이 용이하고 인체조직 제품과는 달리 별도의 이식 기록이나 보고 의무가 없다. 또 0.25g, 0.5g, 1g 등 다양한 용량으로 공급돼 경제적 시술이 가능하다.
제품 문의는 02-550-8869로 하면 된다.